Oxit bazơ là gì? Nó có những tính chất nào đặc trưng và được sử dụng như thế nào? Để hiểu rõ hơn về oxit bazơ bạn đọc hãy cùng VIETCHEM tìm hiểu dưới bài viết dưới đây nhé.
1. Định nghĩa oxit bazơ là gì?
Khái niệm oxit bazơ là gì được hiểu theo cách đơn giản nhất đó là sự kết hợp của một kim loại với nguyên tử oxi và các kim loại.
Ví dụ như Na2O, K2O, BaO…
Công thức oxit bazơ gồm 1 hay nhiều nguyên tử kim loại (M) và một hay nhiều nguyên tử oxi. Tùy thuộc vào hóa trị của kim loại mà có công thức thích hợp như những kim loại có hóa trị 1 cần 2 nguyên tử kim loại để tạo thành oxit bazơ. Kim loại hóa trị 2 thì chỉ cần 1 nguyên tử oxi.

2. Phân loại của oxit bazơ
Tùy thuộc vào kim loại trong phân tử mang những đặc trưng riêng mà nó được phân loại thành những loại dưới đây:
- Oxit bazơ tan: Bao gồm các loại kiềm như Na, K, Li… và kiềm thổ như Na, Sr, Cs, Li, Ba,...
- Oxit bazơ không tan: Bao gồm oxit của các kim loại còn lại, như của Fe, Cu,...
Ngoài ra, dựa vào tính chất mà nó còn chia thành oxit lưỡng tính và trung tính:
- Oxit lưỡng tính: Là những oxit tác dụng được với các dung dịch axit, tác dụng với dung dịch bazơ tạo thành muối và nước. Điển hình là Al2O3, ZnO...
- Oxit trung tính: Là các oxit không phản ứng với nước để tạo ra axit hay bazơ, đồng thời không phản ứng với axit hay bazơ để tạo thành muối. Ví dụ như NO, CO…
3. Tính chất hóa học đặc trưng của oxit bazơ
Oxit bazơ tác dụng với nước, oxit axit, axit cụ thể là:
- Tác dụng với H2O:
Chỉ có oxit bazo của kim loại kiềm và kiềm phổ mới có phản ứng với nước. Vì vậy chúng tan được trong nước, bao gồm: Na2O, CaO, BaO, K2O,... tạo ra bazơ (kiềm) tan tương ứng là NaOH, Ca(OH)2, Ba(OH)2, KOH.
Na2O + H2O → 2NaOH
BaO + H2O → Ba(OH)2
K2O + H2O → 2KOH
Các sản phẩm thu được sau phản ứng là NaOH, KOH,... cho giấy quỳ tím chuyển màu.
- Tác dụng với axit
Hầu hết các oxit bazơ đều phản ứng với axit tạo thành muối và nước. Công thức chung được thể hiện như sau: Oxit bazơ + Axit → Muối + H2O.
Na2O + H2SO4 → Na2SO4 + H2O
CuO + 2HCl → CuCl2 + H2O
- Tác dụng với oxit axit
Một số oxit bazơ cũng phản ứng với oxit axit để tạo thành muối. Thông thường đó là các oxit bazơ tác dụng được với nước như oxit của kiềm, tạo muối tan trong nước. Còn tác dụng với nước tạo muối không tan thường là oxid kiềm thổ.
Công thức như sau: Oxit bazo + Oxit axit → Muối.
Cụ thể như:
Na2O + CO2 → Na2CO3
BaO + CO2 → BaCO3↓

4. Ứng dụng của Oxit bazơ trong cuộc sống
Oxit bazơ rất quan trọng và được ứng dụng nhiều trong thực tiễn đời sống từ việc xử lý nước hồ bơi, sản xuất thuốc, xử lý vải thô,... Cụ thể:
- Công nghiệp hóa chất và dược: Được dùng để sản xuất sản phẩm chứa gốc sodium và làm chất tẩy trắng hay khử trùng.
- Trong phòng thí nghiệm: Là chất hóa học quan trọng để học tập và nghiên cứu.
- Trong ngành thực phẩm: Pha chế dung dịch kiềm, xử lý rau, củ quả trước khi chế biến hoặc đóng hộp.
- Ứng dụng trong ngành công nghiệp dệt nhuộm: Làm chết phân hủy pectins, sáp để xử lý vải thô, giúp vải dễ hấp thụ màu nhuộm và có màu đẹp nhất.
- Xử lý nước, đặc biệt nước trong hồ bơi: Các oxit bazo hòa tan trong nước làm tăng nồng độ pH. Ngoài ra, oxit bazo cũng được dùng để trung hòa và khử cặn bẩn trong đường ống nước sinh hoạt.
- Ứng dụng trong ngành dầu khí: Bazo cân bằng PH cho dung dịch khoan, loại bỏ sulphur và các hợp chất sulphur hay hợp chất axit có trong tinh chế dầu mỏ.
- Trong các nghiên cứu hiện đại, các hạt nano oxit kim loại có rất nhiều ứng dụng như vi điện tử, năng lượng, lưu trữ, khử nhiễm môi trường, cảm biến khí, chế tạo gốm, y sinh…
Ngoài ra, một số oxit quan trọng được ứng dụng trong đời sống như:
- Magie oxit (MgO) - là một chất dẫn nhiệt và cách điện tốt được sử dụng trong gạch chịu lửa và cách nhiệt.
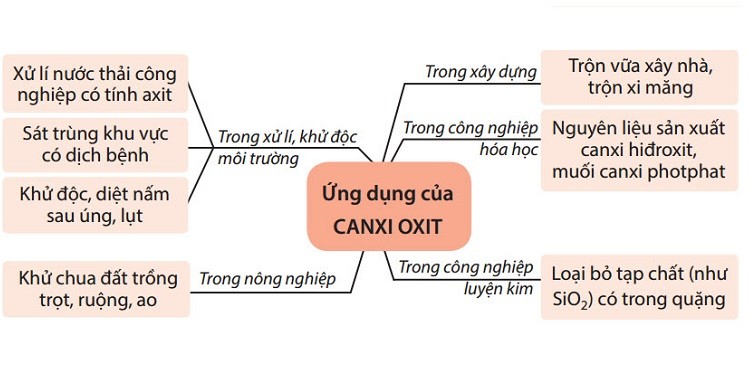
- Một oxit khác là oxit canxi (CaO), còn được gọi là vôi sống được sử dụng rộng rãi trong công nghiệp thép và trong nước thanh tẩy.
- Oxit sắt phổ biến, được sử dụng rộng rãi vì chúng rẻ tiền và đóng vai trò quan trọng trong nhiều quá trình sinh học và địa chất. Con người sử dụng oxit sắt rộng rãi như quặng sắt trong thermite, chất xúc tác, chất màu bền (lớp phủ, sơn và bê tông màu) và huyết sắc tố.
Trên đây là những thông tin cơ bản về oxit sắt. Nếu có bất cứ thắc mắc nào bạn có thể liên hệ với chúng tôi trong thanh chat phía cuối màn hình hoặc tham khảo thêm những bài viết trên toitaigioibancungthe.vn.





![[ CẢNH BÁO] Cách sử dụng nước Kangen đúng cách?](uploads/2020/09/13-1.png)





